原标题:美国将瑞德西韦认证为新冠肺炎“孤儿药”,将独家供给,或许约束拷贝药供给
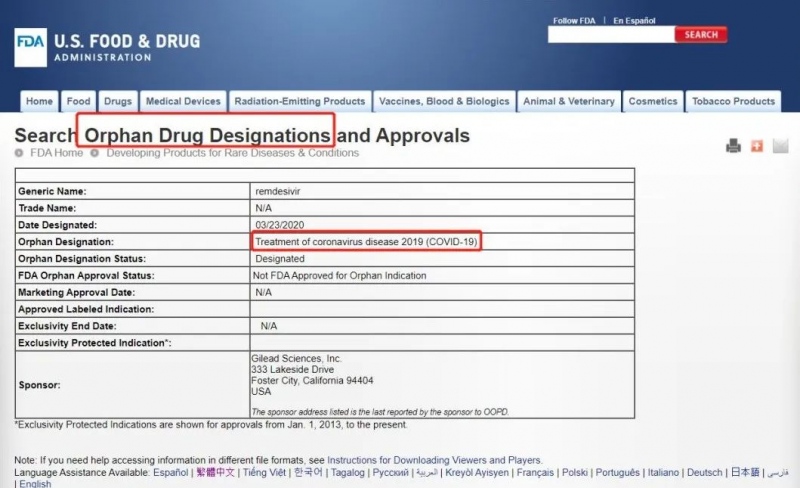
北京时刻3月24日早4:30(美东时刻23日4:30pm),美国食物和药品管理局(FDA)发布音讯:同意认证美国Gilead科学公司的瑞德西韦(Remdesivir)孤儿药认证(Orphan Drug Designations);习惯症为新冠肺炎(COVID-19)。
此举将加快瑞德西韦医治新冠肺炎的临床运用,答应吉祥德公司对瑞德西韦(Remdesivir)独家维护,一起,也会阻挠其他拷贝药出产商供给瑞德西韦拷贝药。
在此之前,美国总统特朗普就呼吁FDA简化其对瑞德西韦(Remdesivir)等药物的同意程序。
瑞德西韦开端是由美国吉祥德公司研制的用于对立埃博拉病毒的试验性药物,它经过按捺一种要害的酶——RNA依靠的RNA聚合酶(RdRP),然后按捺病毒的拷贝。但是,不幸的是,研讨人员在刚果民主共和国的埃博拉病毒医治试验中,瑞德西韦对埃博拉病毒并没什么作用。
山穷水尽的是,美国北卡罗莱纳大学教堂山分校的研讨人员在细胞和动物试验中发现,瑞德西韦能够有用按捺SARS-CoV和MERS-CoV。此外,美国的两例重症患者在接受了瑞德西韦医治后,病况得到显着改进。
因而,瑞德西韦(Remdesivir)被认为是现在最有潜力治好新冠肺炎的一款药物。WHO也于近来将其列为四种最有期望的新冠肺炎医治计划之首。
1月21日,中科院武汉病毒所将
瑞德西韦(Remdesivir)用于抗新冠病毒的用处申报了我国发明专利,此举引发广泛争议。随后,瑞德西韦(Remdesivir)在国内获准展开三期临床试验,由北京中日友爱医院曹斌教授牵头在武汉疫区展开临床试验。
需求着重的是,瑞德西韦医治新冠肺炎现在尚在临床试验中,
尚未在全球任何国家取得答应或同意,其医治新冠肺炎的安全性和有用性尚未被证明。
瑞德西韦即使要以孤儿药的身份上市,也还需求严厉的临床试验流程。什么是孤儿药孤儿药(Orphan Drug),指一些专门用于治好(cure)或医治/操控(treat)稀有病的药物。稀有病指患病人数占总人口0.65‰-1‰的疾病。
因为稀有病患者数量少,新药研制本钱昂扬,因而医药研制公司为了考虑赢利和出资报答,往往不愿意针对稀有病进行巨额研制投入。
为了鼓舞对稀有病的药物,1983年开端美国FDA给针对孤儿症的研讨项目供给绿色通道,加快批阅的进程。孤儿药认证后的优势依据美国1983年发布《孤儿药法案》,FDA为开发“稀有病”疗法的制药公司供给为期7年的商场独占期,且该维护不受专利的影响。
在此期间,该药物仅由原研制企业独家
出产出售,FDA 不再同意其他具有相同习惯证的药物上市,拷贝药品的恳求也将被制止。
此外,还会供给税费优惠方针、专项研制基金赞助、快速审评方针、新药恳求费用革除、帮忙药物的研讨和试验设计等。
因而,此次瑞德西韦(Remdesivir)取得FDA孤儿药认证,对吉祥德科公司的好处是清楚明了的,这将阻挠其他拷贝药出产商供给抗拷贝药。但此举将只答应吉祥德公司对瑞德西韦(Remdesivir)独家维护,因而或许会约束该药物的供给。
此外,因为新冠肺炎疫情在全球范围内的快速增加,对瑞德西韦(Remdesivir)的运用恳求也呈指数增加,面临激增的运用恳求,吉祥德公司暂时放置了对该药品的紧迫运用权。
紧迫运用权是指,在紧迫状况下,现有商场上的产品无法满意需求时,FDA将答应未经FDA批阅的医疗产品或现有医疗产品中未批阅的新运用,用于确诊、医治、防备要挟到生命的疾病或状况。
面临FDA对瑞德西韦(Remdesivir)的孤儿药认证,担任药物专利乱用问题的世界非政府安排Knowledge Ecology International 的担任人James Love表明,《孤儿药法案》是针对稀有病的,而新冠肺炎现已要挟全世界,明显跟稀有病不沾边。
在药品或许缺少的当下,他并不认同FDA对瑞德西韦(Remdesivir)的孤儿药认证。
参阅链接:
https://www.fda.gov/
责任编辑: